講演2|切除不能進行・再発大腸癌におけるがんゲノムプロファイリング検査の“実践”
演者:市川 度 先生(昭和医科大学藤が丘病院 腫瘍内科・緩和医療科)
私からは、より実臨床での “実践” という視点でお話をさせていただきます。

私のおります昭和医科大学藤が丘病院は、2022年6月よりがんゲノム医療連携病院となりました。そこからの約2年半で、200例ほどのがんゲノムプロファイリング検査(CGP検査)を実施しています。
Guardant360 CDxがん遺伝子パネル(以下Guardant360 CDx)は2023年10月より導入し、2025年2月までの間に64例に使用しています。2024年4月までの最初の20例(うち大腸がんは8例)の結果をまとめると、20例中、リキッドCGP検査の結果「推奨治療あり」が6例(30%)、その後治療に移行したのは4例(20%)でした。
大腸がんでは「推奨治療あり」が4例(50%)、治療に移行したのは3例(38%)という結果でした12)。この数字は、私の約40年の臨床経験の勘に基づき治療につながりそうな患者さんだけに実施するという、かなりのセレクションバイアスをかけたものではありますが、臨床試験とは違って実臨床であれば、これだけ高い割合になる可能性があり、十分に活用できるということかと思います。
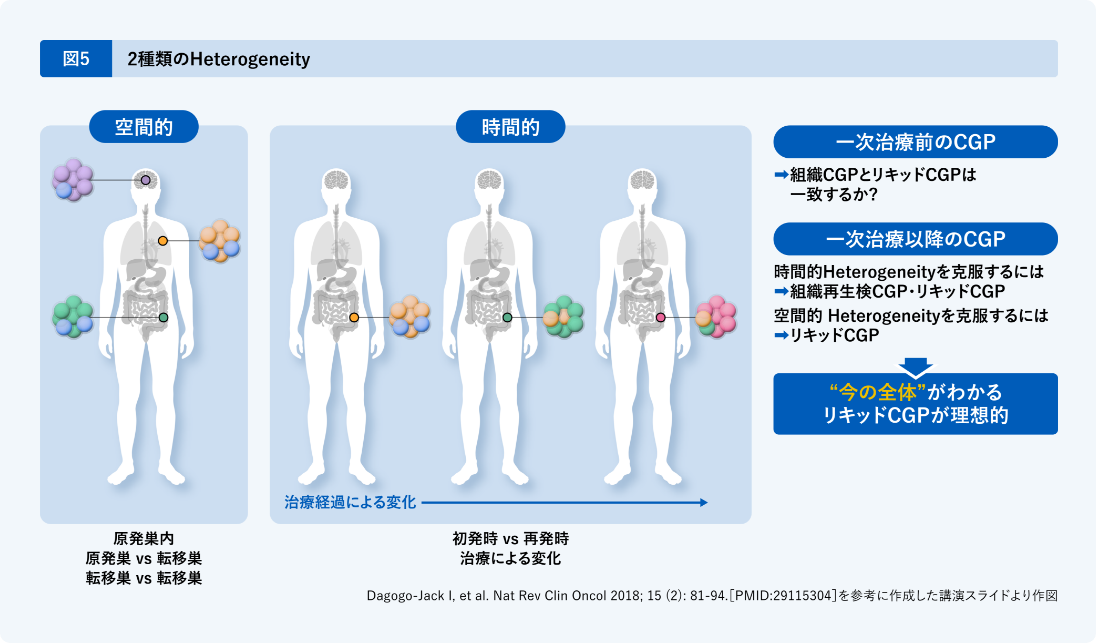
先ほど中村先生からもお話があったように、がんの不均一性(Heterogeneity)は空間的なものと、時間的なものの2つに分かれます(図5)。
空間的なHeterogeneityは、①原発巣内、②原発巣-転移巣間、③転移巣-転移巣間の3つ、時間的なHeterogeneityは、①初発時(手術時)-再発時、②治療による変化の2つがあります。
今の保険制度上CGP検査を実施できる一次治療以降のHeterogeneityを考えると、時間的なHeterogeneityを克服するには、再生検による組織CGPか血液CGPしかなく、また空間的なHeterogeneityを克服するには血液CGPしかありません。
つまり “今の全体” が分かる血液のCGPが理想的である、と私は考えています。現状、保険を使って検査ができるのは1回だけです。
次の治療につながるチャンスをより高くしたい、と考えた時に、Guardant360 CDxは治療に到達するに十分な74遺伝子の解析と、検体中にわずか5ngのセルフリーDNAしか含まれていなかった場合でも多くの検体で遺伝子異常を報告する高い解析性能を持ちますので、私は積極的に使用するようにしています。
実際にリキッドCGPを使用するにあたり、中村先生が監修された3つのポイントは、「病態」、「腫瘍量」、「転移部位」とのことでした(図4)。
このうち「病態」と「転移部位」はシンプルなメッセージで非常に分かりやすいと思います。
ただ、「腫瘍量」については少しイメージしづらいかもしれません。そのヒントになるのが、アルカリフォスファターゼ(ALP)とLDHです。
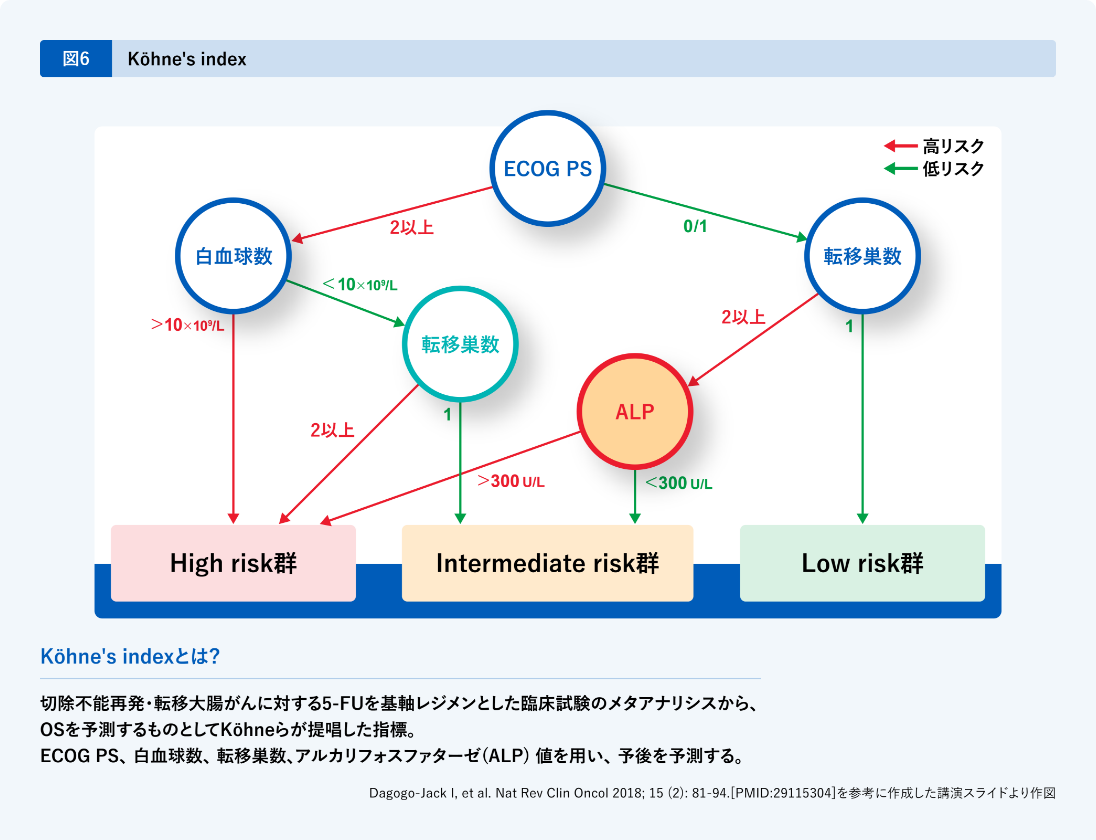
まずALPについてですが、Köhne’s indexが参考になります(図6)。これはALPの他にPSや転移個数、白血球数などから予後を予測するチャート13)で、AOIのグループで作られたものです。
GERCOR studyの結果がもっとシンプルで、de Gramont先生のグループが提唱したPSとLDHだけの指標があります(図7)14)。
2002年と2011年の論文なので若い先生はあまりご存じないかもしれませんが、ALPとLDHは腫瘍量を反映していると以前から言われており、実臨床では参考になると思います。

切除不能・進行再発大腸がんにおけるリキッドCGPのニーズは、大きく分けるとサイエンスからのニーズと、患者・家族・医療従事者のニーズの2つあると考えます。
前者は“今の全体”のバイオロジーを理解することであり、治療がなぜ効いたのか/なぜ効かなくなったのか?ということの答えを得ることにあります。
後者は、やはり治療につなげることだろうと思います。そのためには、希少フラクションを見つけることと、“今の全体”を知ることによって抗EGFR抗体薬のリチャレンジやNeoRASアプローチなどの適切な治療を検討する、ということが現時点での使いどころであろうと考えています。
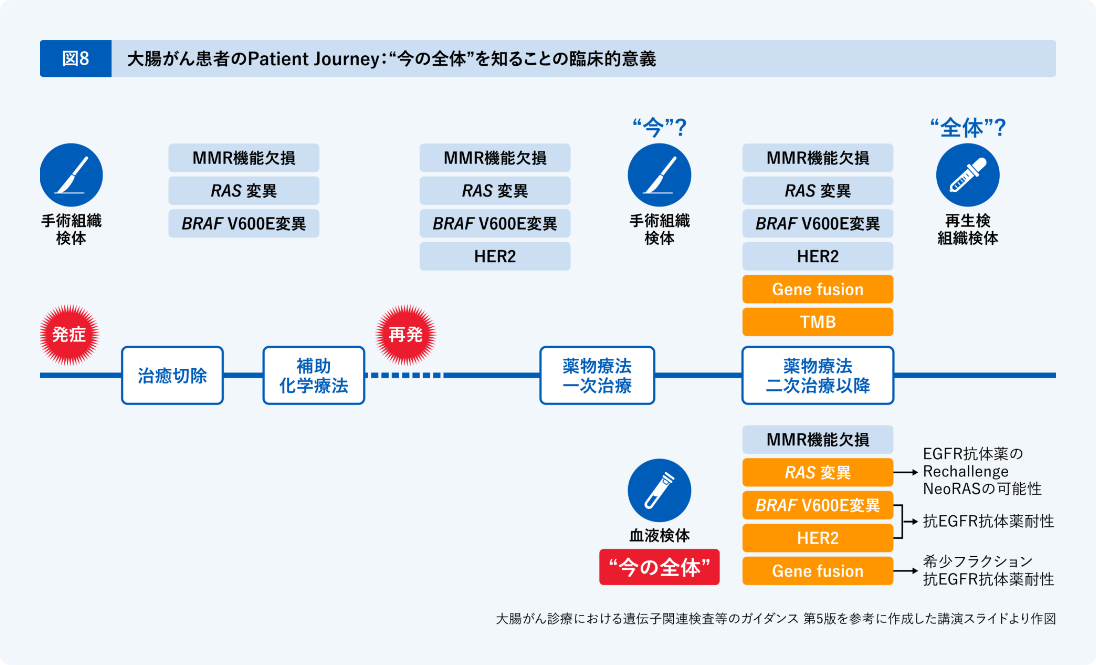
本日の内容を、大腸がん患者さんのPatient Journey上にまとめました(図8)。
切除不能・進行再発大腸がんの治療においては、組織検体を使って一次治療前にMMR機能欠損、RAS変異、BRAF V600E変異、HER2を調べることは、大腸癌治療ガイドラインにも記載されており、いまや必須となっています。
その後CGPを行う際に、リキッドであれば “今の全体”を知ることができ、RAS変異に関しては抗EGFR抗体のリチャレンジやNeoRASアプローチなど適する治療を選択することも可能になります。
また、BRAF V600E変異やHER2陽性といった抗EGFR抗体薬に抵抗性を示すものを確認することによって抗EGFR抗体薬の適切な使用やALKなどのGene fusionを確認することで希少フラクションが見つかり、適した治療につながる可能性があります。
“今の全体”を知ることができ、治療に到達するに十分な数の遺伝子を高性能で解析可能なGuardant360 CDxは、患者さん・ご家族、そして我々医療従事者の拠り所になるものと、私は確信しております。