進行消化器がんにおける血中循環腫瘍DNA(ctDNA)を用いた
リキッドバイオプシーの臨床的有用性:
SCRUM-Japan GI-SCREENとGOZILA study
Clinical utility of circulating tumor DNA sequencing in advanced gastrointestinal cancer:
SCRUM-Japan GI-SCREEN and GOZILA studies
Nakamura Y, et al., Nature Medicine 2020; 26(12): 1859-1864.
著者にガ―ダントヘルス社の社員が含まれている。
● 本試験は、消化器がんを対象とした臨床試験のスクリーニング検査として、リキッドバイオプシーの有用性を組織検査と比較した観察研究です。
試験デザイン
Guardant360®を用いたリキッドバイオプシーの有用性を組織検査と比較しました。
横にスクロールできます →
- 目 的 消化器がんを対象に腫瘍組織検査とリキッドバイオプシーで臨床試験のスクリーニング検査としての有用性を比較する。
- 対 象 2015年2月から2019年4月の期間にGI-SCREENに登録された5,743例(解析対象5,621例)及び、2018年1月から2019年8月の期間にGOZILA studyに登録された1,787例(解析対象1,687例※1)の進行消化器がん患者
- 方 法 GI-SCREENでは、腫瘍組織を採取し、遺伝子パネル検査(LDT)※2を用いてがん関連遺伝子の異常を調べ、GOZILA studyでは、血液を採取し、Guardant360を用いたリキッドバイオプシーで74のがん関連遺伝子の異常を調べた。
- 評価項目 結果報告までの期間、臨床試験登録までの期間、臨床試験登録患者割合、客観的奏効割合(ORR)、無増悪生存期間(PFS)、ctDNAプロファイルなど
- 解析計画 観察研究であり、統計学的な症例数の設定は行わなかったが、GI-SCREENとGOZILA studyの解析対象患者数は、それぞれ5,621例、1,687例であり、30%に治療標的となる遺伝子異常が検出され、うち10%が臨床試験に登録されると仮定した。その結果、期待される登録患者数はGI-SCREENが169例、GOZILA studyが51例となった。GI-SCREENとGOZILA studyの群間比較では、カテゴリー変数の場合はFisherの正確確率検定またはχ2検定、連続変数の場合はMann-Whitney検定を用いた。生存期間はKaplan-Meier法で推定し、群間比較はLog-rank検定で行った。また、Cox比例ハザードモデルを用いてハザード比(HR)と95%信頼区間(CI)を算出した。
- ※1 大腸がん654例、胃・食道腺がん260例、食道扁平上皮がん108例、膵管腺がん363例、胆管がん188例、その他114例
- ※2 腫瘍組織を用いた遺伝子パネル検査(LDT)で、143もしくは161の遺伝子異常の有無を評価した。
Nakamura Y, et al., Nature Medicine 2020; 26(12): 1859-1864.
検査成功率と結果報告までの期間
リキッドバイオプシーでは、組織検査と比べて、結果報告までの期間中央値が22日間短縮しました。
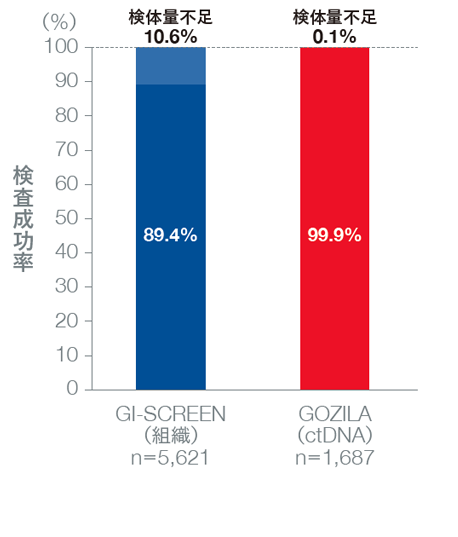
検査成功率はGI-SCREENが89.4%、GOZILA studyが99.9%でした。 登録から結果報告までの期間の中央値はGI-SCREENが33日に対してGOZILA studyでは11日と、GOZILA studyで有意に短いことが示されました(p<0.0001、Mann-Whitney検定)。
検査成功率
結果報告までの期間
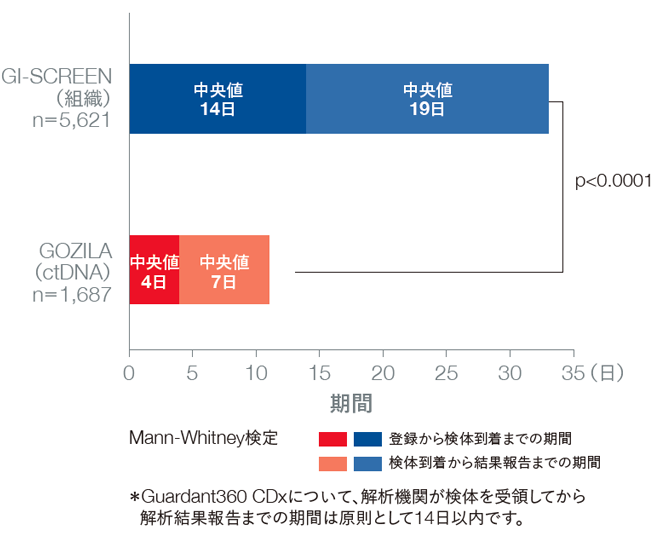
Nakamura Y, et al., Nature Medicine 2020; 26(12): 1859-1864, Springer Nature, reproduced with permission from SNCSC.
臨床試験に登録された患者の割合と推移
リキッドバイオプシーにより臨床試験に登録された患者の割合は組織検査の2倍以上でした。
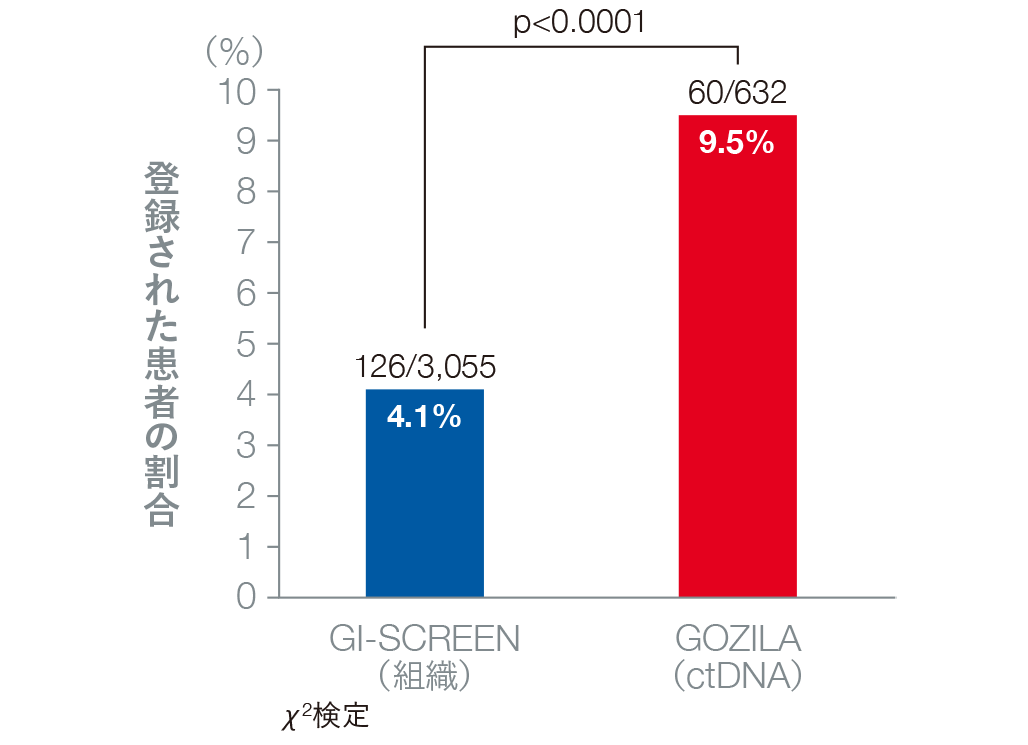
治療標的となる遺伝子異常を有する患者のうち、臨床試験に登録された患者の割合は、GI-SCREENが4.1%、GOZILA studyが9.5%であり、GOZILA studyで有意に高いことが示されました(p<0.0001、χ2検定)。
臨床試験に登録された患者の割合
GOZILA studyにおける登録可能な臨床試験数はGI-SCREENより少数である(11試験 vs. 28試験)にもかかわらず、GOZILA study開始後は1ヵ月あたりの登録患者数が8.1人/月と増加しました。
臨床試験に登録された患者数の推移
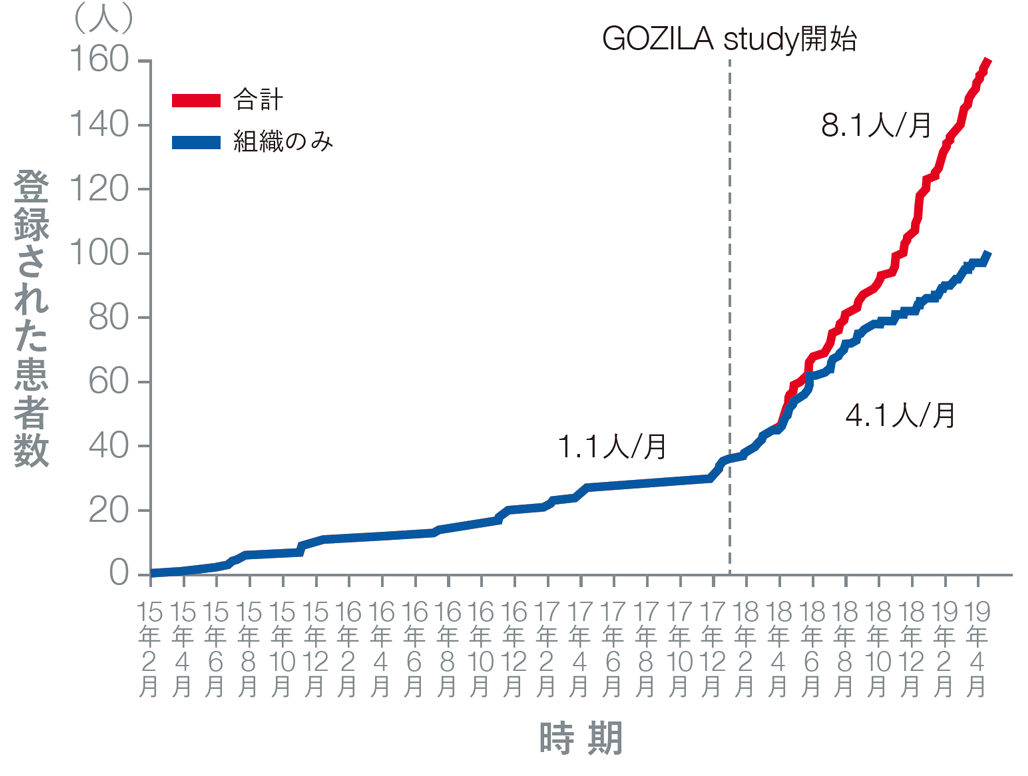
Nakamura Y, et al., Nature Medicine 2020; 26(12): 1859-1864, Springer Nature, reproduced with permission from SNCSC.
治療標的となる遺伝子異常が同定された患者の割合
リキッドバイオプシーでは57.2%の患者に治療標的となる遺伝子異常が同定されました。
治験で検討中のバイオマーカーまで含めると、GI-SCREENでは54.3%、GOZILA studyでは57.2%に治療標的となる遺伝子異常が同定され、GOZILA studyで有意に高値でした(p=0.041、Fisherの正確確率検定またはχ2検定)。
治療標的となる遺伝子異常が同定された患者の割合
横にスクロールできます →
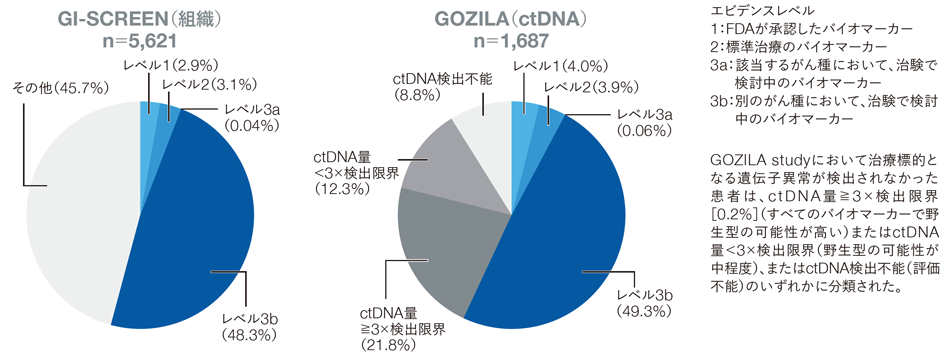
Nakamura Y, et al., Nature Medicine 2020; 26(12): 1859-1864, Springer Nature, reproduced with permission from SNCSC.
客観的奏効割合(ORR)と無増悪生存期間(PFS)
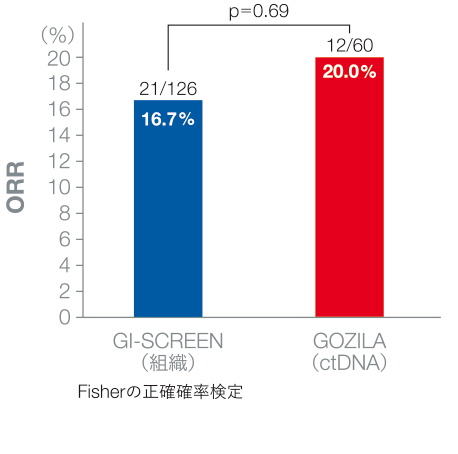
リキッドバイオプシーでスクリーニングした患者群でも、組織検査と同様のORRとPFSが示されました。
ORRは、GI-SCREENが16.7%、GOZILA studyが20.0%であり、有意差は認められませんでした(p=0.69、Fisherの正確確率検定)。PFS中央値も、それぞれ2.8ヵ月、2.4ヵ月であり、有意差は認められませんでした(p=0.70、Log-rank検定)。
ORR
PFS
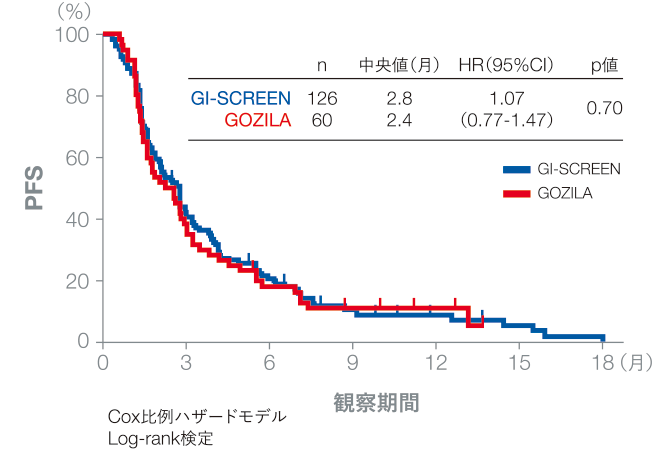
Nakamura Y, et al., Nature Medicine 2020; 26(12): 1859-1864, Springer Nature, reproduced with permission from SNCSC.
臨床試験に関する詳細資料
上記以外にも、製品に関する主要な臨床試験の詳細を解説しています。
進行消化器がんにおける血中循環腫瘍DNA(ctDNA)を用いたリキッドバイオプシーの臨床的有用性:
SCRUM-Japan GI-SCREENとGOZILA study
本試験は、消化器がんを対象とした臨床試験のスクリーニング検査として、リキッドバイオプシーの有用性を組織検査と比較した観察研究です。
進行消化器がん患者のマイクロサテライト不安定性評価における血漿ジェノタイピングの臨床的妥当性:
SCRUM-Japan GOZILAの付随研究
臨床研究GOZILAの付随研究において、PCRによる組織MSI検査を比較対照としてリキッドバイオプシーによるMSI検査の同等性を評価しました。
ERBB2(HER2)遺伝子増幅を有する転移性大腸がんに対するペルツズマブ+トラスツズマブ併用療法の血中循環腫瘍DNA(ctDNA)を指標とした治療:第II相試験
本試験は、リキッドバイオプシーが、組織検査と同様に抗HER2抗体併用療法でベネフィットが得られるHER2遺伝子増幅を有する転移性大腸がん患者の選択に有用であることを示した前向き試験です。
進行非小細胞肺がん患者の血漿および組織を解析対象とした次世代ターゲットシークエンスに関する大規模前向きコンコーダンス研究(LC-SCRUM-Liquid)
LC-SCRUM-Liquidは、リキッドバイオプシーと組織検査の遺伝子異常検出の一致率を評価する臨床研究です。










